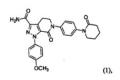
Deze procedure ziet op de stof apixaban, een antistollingsmiddel dat door BMS onder de naam Eliquis op de markt wordt gebracht. Apixaban was in conclusie 1 van het (inmiddels verlopen) octrooi EP 1 427 415 B1 onder bescherming gesteld en is dat in het (nog geldige) ABC 300500. In de kern staat in deze zaak ter beoordeling de stelling van Teva dat dit octrooi nooit verleend had mogen worden, en alsnog nietig moet worden verklaard, waarmee ook het ABC vervalt en de weg vrij komt voor het op markt brengen van het generieke product Apixaban Teva/Sandoz. De rechtbank komt tot het oordeel dat conclusie 1 van het octrooi en daarmee ook het ABC geldig is. Het door BMS tegen Sandoz gevraagde verbod om inbreuk te maken op het ABC wordt dan ook toegewezen.
OCTROOIRECHT
Wat leert de vakpersoon uit de aanvrage?
De vakpersoon begrijpt uit de octrooiaanvraag dat deze zich richt op het ontwikkelen van nieuwe en verbeterde Factor Xa-remmers, met een nadruk op verbindingen die selectief en effectief Factor Xa remmen. De aanvraag beschrijft lactam-houdende verbindingen die beter presteren dan bestaande alternatieven, inclusief een voorbeeldverbinding die later als apixaban bekend wordt. Ondanks dat niet alle verbindingen binnen het brede toepassingsgebied aan de vereiste Ki-waarden voldoen, heeft de vakpersoon genoeg kennis om de relevantie en potentie van de genoemde verbindingen voor Factor Xa-remming te beoordelen.
De aanvraag hoeft niet expliciet experimenteel bewijs te bevatten, omdat het technisch effect als geheel door de technische leer van de aanvraag wordt ondersteund. Daarmee mag BMS voor de octrooiaanvraag gebruik maken van bewijs, ook als dat bewijs pas na de aanvraagdatum is ontwikkeld, om de werking en voordelen van de verbindingen, zoals verbeterde Factor Xa-remming, te onderbouwen.
Inventiviteit ontbreekt wanneer de gemiddelde vakpersoon, uitgaande van de relevante stand van de techniek, het probleem zou - en niet slechts kon - hebben opgelost op de wijze die wordt geclaimd in het octrooi.
De vraag die tot slot beantwoord moet worden is dan ook of de gemiddelde vakpersoon, startend vanuit WO 131, zonder inventieve denkarbeid tot de selectie van de in conclusie 1 opgenomen lactam-houdende verbinding (apixaban) zou komen. BMS heeft gemotiveerd betwist dat daarvoor aanwijzingen (pointers) bestaan en onderbouwd dat meerdere stappen moeten worden gezet. Teva heeft haar stellingen dat de vakpersoon zonder inventieve denkarbeid vanuit WO 131 - al dan niet in combinatie met WO 191 - tot apixaban zou komen na die gemotiveerde betwisting niet meer gehandhaafd. De conclusie moet dan ook zijn dat de vakpersoon niet zonder inventieve denkarbeid zou komen tot de in conclusie 1 opgenomen verbinding.
De eerste grondslag van Teva voor de nietigheid van het ABC (art. 15 lid 1 aanhef en sub c ABC-Vo) slaagt niet. Los van de geldigheid van het octrooi, heeft Teva nog aangevoerd dat het ABC niet geldig is op grond van het Royalty Pharma-HvJ EU-arrest omdat Apixaban na de prioriteitsdatum van EP 415 zou zijn ontwikkeld. Die stelling slaagt evenmin. In de eerste plaats mist deze feitelijke grondslag omdat uit de stukken blijkt dat apixaban voor de prioriteitsdatum was ontwikkeld en getest.
De rechtbank wijst de vorderingen van Teva af.
In de zaak tegen Sandoz dient zij iedere directe en indirecte inbreuk op ABC 300500 in Nederland te staken en gestaakt te houden en veroordeelt Sandoz tot schadevergoeding. Opgaveplicht. Recall.
IEPT-versie volgt later